The source-page: http://people.csail.mit.edu/seneff/statins_muscle_damage_heart_failure.html
tarafından Stephanie Seneff
1. Giriş
Statin uyuşturucu kullanımı giderek nedeniyle kolesterol düşürme kalp hastalığı önlemede önemli bir adım olduğunu yaygın inanışın, son birkaç on yıl içinde artmıştır. Statinlerin etkili olduğu yadsınamaz: bunlar bir kaç hafta normal aralık içinde bir oyuğa 300 db/ml serum kolesterol seviyelerini azaltır. Zaten normal kolesterol düzeyleri bulunan bir kişi için, statinler doğada görülmeyen seviyelere onların kolesterol buraya gelebilirim. Statinler ayrıca azaltmak gösterilmiştir göreceli kalp krizleri nüfusun bu segment için oldukça nadir olduğu için, hem 30% varan oranlarda tarafından onların 50 erkeklerde kalp krizi riskini ama, mutlak risk azaltma yalnızca düzeyindedir 2%, genellikle kişi, tedavi edilen kaçırılan bir nokta.
Bütün ilaçlar potansiyel yan etkileri vardır ve herhangi bir ilaç ile ilaç garanti olup olmadığına karar vermek risk/yarar faktörlerini değerlendirerek meselesi. Statin ilaçlar bilişsel ve bellek bozukluğu, libido azalması, ve kas ağrısı ve halsizlik içeren yan etkiler, bir dikkat çekici ölçüde çeşitli belirledik. ilaç üreticileri yan etkilerin görülme sıklığı oldukça nadir olduğunu iddia, ama çoğu zaman yan etkiler birkaç ay veya tedavi içine hatta yıllar sonrasına kadar görünmez. Bu vakaların çoğunda, statin ilacı sorunun nedeni olduğu açık olmayabilir. Bu yan etkileri kolayca artan yaşla isnat edilebilir, çünkü bu özellikle doğrudur. Aslında, daha sonra gösterir şekilde statin yan etkiler iyi yaşlanma sürecinin hızlandırılması şeklinde yorumlanabilir.
Bana göre, statin ilaçlar yan etkileri riske değer asla. Kolesterol memeli hücreleri yaşayamaz onsuz hayati besin vardır, ve o zamandan iyi bir fikir olabilir kolesterol sentezleme vücudun yeteneğini sakatlanma bana düşünülemez. 2009 yılında yayınlanan bir mükemmel ve son derece bilgilendirici derlemede, Wainwright vd. “Tepeden tırnağa”. Hücre zarının bir istikrarsızlığa yol, kolesterolü tüketerek, statin ilaçları güçlü bir argüman geliştirdiklerini Bu sorun da, ciddi sağlık koşulları ve hastalıklar dahil diyabetin uzun listeye riskini artırır , multipl skleroz, bilişsel sorunlar, hemorajik felç, kanser, ve hatta ALS (aynı zamanda Lou Gehrig hastalığı olarak da yaygın olarak bilinen amyotrofik lateral skleroz). Onların argümanlar 85 hakemli dergi yayınlara referanslar tarafından desteklenmektedir. Ben statinlerin risk artabilir önceki yazılarda savundular Alzheimer hastalığı, yanı sıra sepsis, kanser ve kalp yetmezliği.
Statin tedavisi için en yaygın olarak rapor edilen yan etkiler, kas ağrısı, halsizlik vardır. Kontrolsüz bırakılırsa, bu semptomlar rabdomiyoliz (şiddetli kas hasarı) ve böbrek yetmezliği gelişebilir. nefes almada zorluk yol açabilir akciğerlerde kas güçsüzlüğü; kalbinde kalp yetmezliğine yol açar. Statin kullanıcıların karaciğer ve kas enzimleri çok yüksek yükselmeye eğer statin tedavisine durdurmak anlamına onların doktorlar sayesinde çok rahat. Ancak uygulamada, bu (statin tedavisi durdurulduktan sonra sorun gitmez) geri dönüşü olmayan kas hasar mümkündür, ve enzim düzeyleri normal aralığın üzerinde olmadığında bu bile gerçekleşebilir.
Bu makale zamanla bir statin kullanıcı majör sakatlık noktasına bazı durumlarda, gittikçe zayıf hale gelebilir neden için bir argüman gelişecektir. Önemli bir mesaj kasları yeterli enerji elde etmek kendilerini yediklerini zorunda olmasıdır. Ama başka bir faktör hücre duvarlarının daha sonra parçalanması ile kas dokusuna oksidatif hasar, bir. Bu iskelet kasları için değil, aynı zamanda solunum ve kalp kası kontrol eden solunum kasları için sadece doğrudur. devamı kötüye ile, kas hücreleri parçalanır ve döküntü böbrek yetmezliğine yol açabilir böbrekler, kan akımı içinde hareket eder.
Aşağıdaki gibi bu denemenin kalanı ortaya çıkacak. Bir sonraki bölümde, onlar sentez kolesterol değil, aynı zamanda hücre metabolizmasında rol oynayan diğer önemli biyolojik maddelerin sadece müdahale neden de gösterileceği, nasıl çalıştığını statin ilaçlar açıklayacağız. Aşağıdaki bölümde hasar kas hücrelerini statinler delil sunacak. Bölümler 4 ve 5 kasları özellikle aşırı egzersiz gibi stres durumlarında, hareketini etkilemek için yeterli enerjiye sahip olmasını temin ederek katılan biyokimyasal yolları açıklar. Bölüm 6 aşırı egzersizle aynı zamanda statin ilaçların yol açtığı rabdomiyoliz olarak bilinen durumun, ve böbrek yetmezliğine sonraki riskini açıklamaktadır. Bölüm 7, miyoglobin rolü, kas hücrelerinde bulunan önemli bir proteini tarif hastalık sürecinde oynar. Kolesterol oksidatif hasarı hücre zarlarını korur açıklayan bir bölüm sonra dört sonraki bölümler (bölümler 9-12) sırasıyla kaslar, kalp, akciğerler, pankreas, statin hasar yankıları ayrılacaktır. Sonuç bölümünde ise kompozisyon özetlemek değil kas hasarına başına ama beyne gelen sinyalleri ileten omurilikteki motor nöronların hasarı nedeniyle ALS, fiziksel olarak devre dışı bırakılması nörodejeneratif hastalık benim yaklaşan denemesinde dair ipuçları verecektir iskelet kaslarına.
2. Statin İlaçların Biyolojik Mekanizması
Neden statinler kadar çok yan etkilere neden yok? Bu soruyu cevaplamak için kolesterol vücut hücrelerinin bütünlüğünü ve işleyişini sürdürmek oynadığı tüm önemli roller açıklayan gerektirir. Ancak, statinler kolesterol sentezi ile değil, aynı zamanda tüm hücrelerde enerji metabolizmasında önemli bir rol oynar bir enzim, koenzim Q10 sentezi ile sadece engel. Her iki kolesterol ve koenzim Q10 A eksikliği, zamanla potansiyel sağlık sorunlarının büyük bir listeden yol açar. Tam bir birey yanıt verir genetik makyaj bağlıdır nasıl: Bir eksikliği ile karşı karşıya, vücut belirli diğer hücre tiplerini korumak için belirli hücre tiplerini feda etmeye karar verecektir. Beynin nöron feda çünkü Yani, bir kişi Alzheimer gelişebilir, kalp yetmezliği veya rabdomiyoliz (iskelet kas kaybı) için başka succumbs ederken.
Statinler kolesterol sentezine yol açar çok adımlı biyolojik yolun kritik erken adım 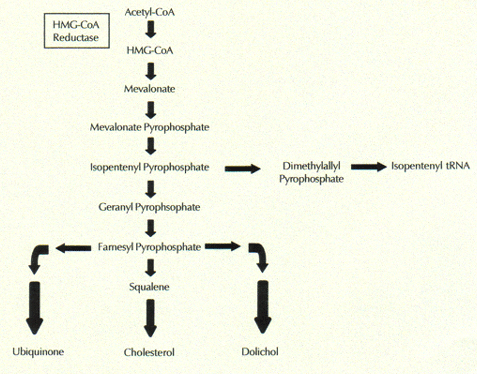 bastırmak. Statinler dramatik kolesterol kan serumu seviyelerini düşürmek edebiliyoruz nedeni budur. Spesifik olarak, statinler üretimini katalize eden enzim olan HMG-koenzim A redüktaz, üretimine müdahale mevalonata kendi ön, HMG-Koenzim A dan.
bastırmak. Statinler dramatik kolesterol kan serumu seviyelerini düşürmek edebiliyoruz nedeni budur. Spesifik olarak, statinler üretimini katalize eden enzim olan HMG-koenzim A redüktaz, üretimine müdahale mevalonata kendi ön, HMG-Koenzim A dan.
Çeşitli daha fazla adım mevalonatın gelen kolesterol üretir. Mevalonat da hücre fonksiyonları için önemli olan diğer biyolojik olarak aktif bir molekül çok sayıda ön-madde olan. sağa doğru, şekil de gösterildiği gibi, antioksidanlar, koenzim Q10 ve dolikoller içerir.
Sözde “kötü” kolesterol, LDL, karaciğerden vücudun tüm hücrelerine kolesterol, yağ ve antioksidanlar sunar. Tüm hücreler, hem yağlar ve kolesterol dış hücre duvarında değil, aynı zamanda çekirdeğini örten zarda da sadece sağlıklı membranlar korumak için mitokondrinin (enerji birimleri üreten) ve lizozomlar (hücrenin sindirim sistemini) gerekir. Antioksidanlar oksijene maruz enerji gıda kaynakları ile oksijen arasındaki kimyasal reaksiyon yoluyla mitokondride oluşturulur her zaman bir sorun zararlı etkilerini nötralize etmek için kritiktir.
Bir çift kör, plasebo kontrollü bir çalışmada ‘de, statinlerin kadar 40% oranında koenzim Q10 serum seviyelerini azaltabildiğini gösterilmiştir. Koenzim Q10 sadece güçlü antioksidan değil, ama aynı zamanda, karbon dioksit ve su elde etmek için, oksijen varlığında glikoz parçalayan sürecinde önemli bir rol oynar. Esas olarak yakıt olarak glikoz yanma olan bu metabolik sentez yolu, iyi bilinen, sitrik asit ya da Krebs döngüsü ile mitokondrilerde gerçekleşmektedir. Bu işlem vasıtasıyla salınır enerji, ATP (adenosin trifosfat), tüm hücreleri, enerji rezervi depolamak için kullanılacak para şeklinde paketlenir.
Dolikoller için özel bir rol oynamaktadır lizozomlar. Lizozomlar onlar kullanışlı malzemeler olarak geri kazanılabilir, böylece hasarlı hücre parçaları enkaz yıkmak için sindirim enzimleri ihtiva “odalar” örülerek kapatılmıştır. Sindirim enzimleri düzgün çalışması için Lizozomlar amacıyla yüksek asitli iç ortam sağlamak zorundadır. Dolikoller yüksek asitli tutmak için lisosomlara hidrojen iyonlarının pompalama sorumludur.
Statinler hücrelere zarar anlamına Son bir yolu onların giriş mekanizması geçer. Statinler “amfifilik” ilaçlar, nispeten büyük olmasına rağmen hücre duvarının kırmaya yönetmek adı verilen bir ilaç sınıfına aittir. Bunlar esas olarak hücre zarı bir bölümünü çözülmesiyle bir sabun gibi hareket ederler. Bu temizlenmiş ve lizozomlar ile geri gereken bir yamalı gereken duvar, delik, aynı zamanda enkaz bırakır. Deliğe yama için olan tedarik ölçüde statin ilacı nedeniyle azalır LDL parçacıklarının gelen hem yağ ve kolesterol yeni kaynaklar gerektirir. Hücre statin ilacı molekülleri tarafından tanıtılan tüm delikleri onarmak için yüzden zamanla giderek daha zor hale gelir. Hücre duvarı amfifilik ilaca bağlı bir önceki maddelere daha geçirgen hale geldikçe.
3. Statinler, Kas Ağrısı, Halsizlik Ve Rabdomiyoliz
Kas hücreleri kişinin tedavi programının bir parçası olarak bir egzersiz rejimi koymak olmuştur, özellikle muazzam enerji ihtiyaçları vardır. Kalp, özellikle, aittir asla. Bu en azından her saniyede oranında 24×7 yenerek devam zorundadır. Bu nedenle kalp ATP bu sözleşmeleri ve bir bölmeden diğerine ve aort üzerinden kan iter her tüketilen doldurmak için koenzim Q10 özellikle bağlıdır.
İlaç kolaylıkla statin tedavisi, bazı durumlarda, kas ağrısı ve/veya kas zayıflığı neden olabileceğini kabul eder, fakat bu yan etkilerin sıklığı, 2% mertebesinde, küçük olduğunu iddia ederler. Bununla birlikte, gözlem çalışmaları Statin kullanan en 10%, 15% kas ağrısı şikayetçi olduğunu göstermiştir. Birçok kişi bu potansiyel yan etkidir farkında oldukları için deneyim ağrı veya güçsüzlük, ancak çok daha büyük olması muhtemeldir gerçek sayı. Semptomlar dayanılmaz hale gelmeden önce Dahası, bazen kümülatif statin hasar birkaç yıl sürer. İnsanlar genellikle kendi ağrıları ve genellikle durumun zayıflatıcı yaşlanıyoruz basitçe nedeniyle olduğuna inanıyoruz hazırız.
Nispeten iyi huylu genel toplum tarafından tepki kas ağrısı üzerinde WebMD tarafından gönderildi makalesinde sorun genel olarak kabul edilmiştir çok daha kötü olduğunu göstermektedir. 200’ün üzerinde sık sık uzun yorumlar pek çok üzücü hikayeleri anlatmak; genellikle doktor da yanlış bilgilendirilmiş ve ağrı statin ilacı nedeniyle olabileceğini reddedildi. Önümüzdeki örneklerden bu anlatılan The New York Times makalesinde. Kansas Bir kadın kolesterolü düşürmek için yıllarca bir statin alarak edilmişti. Aynı süre içinde, o ne de doktoru ne statin tedavisi atfedilen kronik kas ağrısı yaşadı. Hatta işe yaramaz bir omuz operasyonu yol açtı. Onun sorunu, sonunda onun dağılmakta kaslar tarafından salınan yan ürünleri toksik proteinin bir tepki neden olduğu deri lezyonları dönüştü. O deri lezyonları, başka Yanlış teşhisi tedavisi için bir antifungal verildi. Ama statinlerin ile etkileşim antifungal ayrıca onun kas bozuklukları şiddetini arttırmak. Üç ay sonra, o ancak duramazdı ve onun pulmoner kasları nefes alamadığından zayıf idi. O kısa bir süre sonra öldü.
Rabdomiyoliz kasları hızla sık, örneğin, fiziksel travma, bir kaza sonrasında, bir yaralanma nedeniyle parçalanır bir durumdur. Ancak rabdomiyoliz Statin nadir bir yan etkisi olan – kas ağrısı, halsizlik aşırı esas itibariyle burada. Bazı insanlar ciddi rabdomiyoliz ile statin tedavisine hemen tepki ve akut böbrek yetmezliği (ABY) için, genellikle ölümcüldür. Miyoglobin büyük miktarlarda kas hücrelerinden kapalı sloughed ve böbrekleri boğan ve onları tamamen kapatmaya neden olmaktadır. Statin tedavisi başlatma dolayısıyla Rusça rulet gibi biraz – bir tek statin dozu rabdomiyoliz neden olduğu bilinen bir durum da vardır. 31 kişi daha sonraki rabdomiyoliz gelen öldükten sonra statinlerin biri olan Baycol, aniden, 2001 yılında piyasadan çekildi.
4. Kaslar Onların Enerji Kaynağı Nasıl Bakım
Bu bölümde ve sonraki, ben o kas hücrelerini temin katılan metabolik yollar sözleşme için yeterli enerjiye sahip anlatacağız. Oksijen mevcut olduğu, ve güvenli bir şekilde yararlanılabilir zaman, kas oksijen tüketerek, karbon dioksit ve su haline dekompoze besin kaynakları zaman. Ama oksijen, Hayat veren ederken, aynı zamanda çok tehlikeli bir maddedir ve işlem planına göre tam olarak düzenledi değilse nedeniyle oksijen ile tepkimeye yanlış maddelere hasar görme bir sürü olabilir. Oksijen ara belleğe ve mitokondri hücre duvarından iletmeden sorumludur sonra miyoglobin, göreceğiniz gibi, teminat hasar çok alır. Bu aerobik metabolizma süreci, solunum adlandırılan ve mitokondri adı verilen özel organelleri içeride yer alır.
Oksijen yetersizdi, ya da mitokondri işlevsel ise, hücre, hücrenin ana bölme içinde, oksijenin yokluğunda, meydana enerji üretmek için alternatif yollar (örneğin, fermantasyon), sahip olduğunda, sitoplazma olarak adlandırılan. Bu süreçler kas ve karaciğerde arasındaki besin alışverişini gerektirir ve bunlar daha sonra kan akışında göstermek özel enzimlerin yardımı gerektirir. Bunlar, konsantrasyonlar, bir statin ilacı kasları zarar vermiş olup olmadığını tespit etmek için izlenir aynı enzimlerdir.
Bütün bu süreçlerin nasıl çalıştığını detayları bilmek zorunda hissetmeyin, bu bölümü ve bölümü 5 atlayın ve, bence, hala Hikayenin geri kalanını takip edebilecektir olabilir.
Nasıl statinler hasar kasları açıklamak amacıyla, ilk kaslar enerji ihtiyaçlarını yönetmek nasıl açıklamak gerekir. Kaslar sözleşme enerji önemli miktarda gerektirir ve bunlar gıda kaynaklarından başlangıçta elde edilen yağ asitlerini ve glikoz parçalayarak bu enerjinin büyük olsun. Tüm ökaryotik hücrelerde (bir çekirdek içeren hücreler) gibi, kas hücreleri, hücre olarak adlandırılan mitokondri özel bir enerji üreten içinde alt tecrit edilirler aerobik (oksijen-gerektiren) süreçlerle enerji çok üretmek mümkündür. Bu, aerobik metabolizma glikoz, her bir molekül için ATP (adenosin trifosfat) en çok 30 adet yaratarak oldukça etkilidir. Kolayca işlemde depolanan enerjiyi serbest, AMP (adenozin monofosfat) için ayrılmış olabilir, çünkü ATP, enerji birimi olarak düşünülebilir.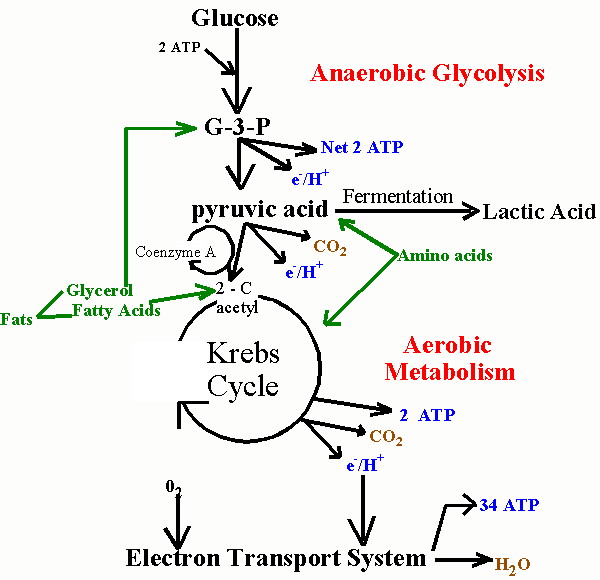
Ne yazık ki, enerji için gıda kaynaklarının metabolize süreci oldukça karmaşıktır. Bir (üstte, sağda) kimyasal reaksiyonlar ve diğer (aşağıda, solda) gösterir katılmaktadırlar hücrenin bölgelerini şematize tamamlayıcı yollarla, gıda metabolizmasını tasvir iki resim bulduk. Bunlar biraz farklı terimler listesine ama gerektiğinde onları birbirine bağlamak için çalışacaktır. Glukoz ilk olarak hücre (insülin yoluyla gerçekleştirilir) girdiğinde, (hücrenin ana bölme) hücrenin sitoplazmasında piruvat (aynı zamanda piruvik asit) dönüştürülür. Bu işlem, ATP, az miktarda serbest bırakır, fakat oksijen yetersizdi olduğunda yararlı hale getirir oksijen, gerektirmez. Piruvat laktat (laktik asit olarak da anılır) (aşağı kırılabilir fermantasyon, oksijen mevcut olmayan ve sitoplazmada aşağıdaki şekilde) ‘de, herhangi bir oksijen gerektirmeden, sözde anaerobik ek enerjiyi serbest bırakmak için, metabolizma. Bu yol, oksijen temini tükenmiş hale aşırı egzersiz, koşullarında kas hücreleri için önemlidir.
Olarak ATP birden fazla yoldan sevk iyi bilinen bir işlem mitokondri (şekilde büyük oval mor biçimli nesne) da gerektirir ve içeren bir çok daha fazla miktarda üretmek için 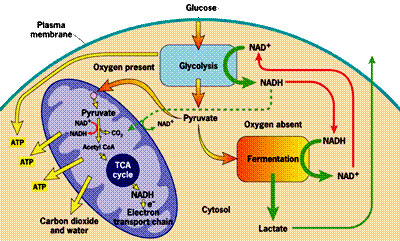 solunum ya da elektron taşıma zinciri, Trikarboksilik asit (TCA) döngüsü ve Krebs döngüsü (TCA döngüsü, oksijen mevcut soldaki şekilde, Krebs döngüsü, aerobik metabolizma yukarıdaki şekilde). Oksijen molekülleri (O için, bu işlem zor2) birbirinden ayrılır edilmesi gerekir, ve ara ürün aşamaları sırasında, tehlikeli serbest radikaller etrafında yalan (bireysel olumsuz henüz tam olarak hidrojen ile birlikte değil oksijen atomu yüklü (H+) meydana getirmek üzere çok stabil bir molekül, su (H2O)). Bu serbest radikaller, çok reaktiftir. Antioksidanlar bu serbest radikalleri emme ve onları zararsız hale getirir olabilir bileşiklerdir. Elektron taşıma zinciri önemli bir rol oynayan iki önemli antioksidan koenzim Q10 (aynı zamanda ubikinon olarak da bilinir) ve sitokrom c vardır.
solunum ya da elektron taşıma zinciri, Trikarboksilik asit (TCA) döngüsü ve Krebs döngüsü (TCA döngüsü, oksijen mevcut soldaki şekilde, Krebs döngüsü, aerobik metabolizma yukarıdaki şekilde). Oksijen molekülleri (O için, bu işlem zor2) birbirinden ayrılır edilmesi gerekir, ve ara ürün aşamaları sırasında, tehlikeli serbest radikaller etrafında yalan (bireysel olumsuz henüz tam olarak hidrojen ile birlikte değil oksijen atomu yüklü (H+) meydana getirmek üzere çok stabil bir molekül, su (H2O)). Bu serbest radikaller, çok reaktiftir. Antioksidanlar bu serbest radikalleri emme ve onları zararsız hale getirir olabilir bileşiklerdir. Elektron taşıma zinciri önemli bir rol oynayan iki önemli antioksidan koenzim Q10 (aynı zamanda ubikinon olarak da bilinir) ve sitokrom c vardır.
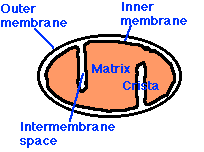 Solundaki küçük şekil bir mitokondri bir şemasını göstermektedir ve aşağıdaki daha büyük bir şekil de hücrenin enerji ihtiyacının büyük bir kısmını üreten, mitokondri çevreleyen duvar boyunca yer alan elektron taşıma zinciri işlemin daha ayrıntılı bir açıklama göstermektedir süreci. Elektron taşıma zinciri protonlar (H enjekte+ esas sonra dönüştürme işlemini tamamlamak için bir pil (membran boyunca yük farkı) yaratarak arası boşluğa) yenilenmiş bir enerji kaynağı olarak geri ATP’ye AMP (kullanılmış). Daha sonra koenzim Q10 yetersiz bir kaynağı (aynı zamanda “ubiquinone” olarak bilinen, şekilde “S”), varsa
Solundaki küçük şekil bir mitokondri bir şemasını göstermektedir ve aşağıdaki daha büyük bir şekil de hücrenin enerji ihtiyacının büyük bir kısmını üreten, mitokondri çevreleyen duvar boyunca yer alan elektron taşıma zinciri işlemin daha ayrıntılı bir açıklama göstermektedir süreci. Elektron taşıma zinciri protonlar (H enjekte+ esas sonra dönüştürme işlemini tamamlamak için bir pil (membran boyunca yük farkı) yaratarak arası boşluğa) yenilenmiş bir enerji kaynağı olarak geri ATP’ye AMP (kullanılmış). Daha sonra koenzim Q10 yetersiz bir kaynağı (aynı zamanda “ubiquinone” olarak bilinen, şekilde “S”), varsa 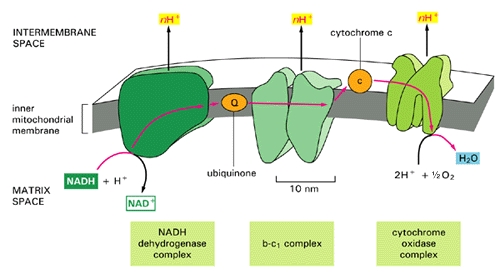 elektron taşıma zinciri olarak etkin bir şekilde çalışmaz. Hidrojen iyonları bunları geri itmek için enerji çok daha büyük bir harcama gerektiren, pasif bir işlem yoluyla mitokondri sızacaktır. Pil şarj azalacak ve oluşturulabilir ATP miktarında bir azalma söz konusu olacaktır. Net etki, üretilen enerji ile ilgili olarak, yetersiz oksijen etkisi çok benzer olacaktır. Bunun yerine mevcut olma, oksijen mevcut olduğu, fakat sadece kısmen suya dönüştürülür, Ancak, çok fazla zarar verici olacaktır (2H+ + 1/2 O2 -> H2 şeklin sağ O), yana olaylar zinciri “q” konumunda kadar tutulur. -OH, H gibi oksijen içeren çeşitli yüksek derecede toksik yüklü iyonlar, O2 (hidrojen peroksit) ve* OH dinlenmeye ve daha sonra göreceğiniz gibi, kas hücre büyük hasara yol.
elektron taşıma zinciri olarak etkin bir şekilde çalışmaz. Hidrojen iyonları bunları geri itmek için enerji çok daha büyük bir harcama gerektiren, pasif bir işlem yoluyla mitokondri sızacaktır. Pil şarj azalacak ve oluşturulabilir ATP miktarında bir azalma söz konusu olacaktır. Net etki, üretilen enerji ile ilgili olarak, yetersiz oksijen etkisi çok benzer olacaktır. Bunun yerine mevcut olma, oksijen mevcut olduğu, fakat sadece kısmen suya dönüştürülür, Ancak, çok fazla zarar verici olacaktır (2H+ + 1/2 O2 -> H2 şeklin sağ O), yana olaylar zinciri “q” konumunda kadar tutulur. -OH, H gibi oksijen içeren çeşitli yüksek derecede toksik yüklü iyonlar, O2 (hidrojen peroksit) ve* OH dinlenmeye ve daha sonra göreceğiniz gibi, kas hücre büyük hasara yol.
elektron taşıma zinciri içinde faaliyet enzimleri kodlayan genlerdeki mutasyonları içeren ender bir genetik bozukluk vardır. Koenzim Q10 bunlardan biridir çünkü özellikle bizim haberle ilgili, ben enzimler Kompleksi yer alır. İlginç bir vaka çalışması NADH- Koenzim Q10 kompleksi ile ilişkili olduğu tespit edilen bir kusur giden bir genetik mutasyon muzdarip her ikisi de üzerine kız kardeş, içeriyordu. tahmin edilebileceği gibi, bunlar (işlem yukarıda tarif edilmektedir), solunum metabolizması oranlarını azaltarak, esas acı. Onlar da son derece zayıf ve egzersiz intoleransı işaretlenmiş almıştı. Onlar icra zaman, laktat ve pirüvat onların seviyeleri, kanda hızla yükseldi.
5. İşletme Enerji Aşırı Egzersiz Sırasında İhtiyaçları
Sağlıklı bir kişinin böyle bir 500 metre bayrak çalışan gibi aşırı egzersiz, yaşar zaman, kaslar kendi enerji ihtiyaçlarını karşılamak için yeterli ATP ile gelip zorlanmaktadır. Hem oksijen ve glikoz tükenmiş olabilir. Bu yetersizlikleri dengelemek için, kas hücreleri sitoplazmadaki yerine mitokondri faaliyet stratejileri, karmaşık bir dizi geliştirdiler. Onlar Statin ilaçlar kasları ve/veya karaciğer zarar belirlemek için izlenir enzimlerdir beri, bizim hikaye sonra yeniden ortaya edecek enzimlerin bir dizi içerir.
Zaten gördüğümüz gibi, tek seçenek (oksijen tüketen olmadan) anaerobik olarak laktik asit üretmek için, ama bu yine de mitokondri meydana gelen aerobik süreç olarak sadece 1/6 kadar ATP sağlar. ATP enerji üretme yöntemi iki aşamada gerçekleşir: ATP ilk ADP (adenozin difosfat) ve son olarak AMP (adenozin monofosfat) dönüştürülür. AMP aşırı miktarda kas hücresi birikir, hücre karaciğer verimli daha yeniden sürece yakında kanda (glikoz) dolabilir, hangi ekstra glikoz almaya indüklenir. ADP bir enzim, kreatin kinaz yardımıyla geri ATP dönüştürülebilir. Buna ek olarak, laktat (glikoz anaerobik oluşturulmuş) piruvat dönüştürülmesi başka enzim da, laktat dehidrojenaz gerektirir. Oksijen yetersiz olduğu zaman Laktat, kurar ve kan akışına salınır. Neyse ki, kalp aşırı egzersiz zamanlarında özellikle önemli hale gelmektedir alternatif yakıt kaynağı, olarak laktat kullanabilmektedir.
Daha fazla glikoz oluşturmak için karaciğer amacıyla, bir alt-tabakayı gerektirir. Kısa vadede, kaslar bu substratı sağlayabilmektedir, ancak kendine cannibalization gerektirir. Açlık kısa süreler boyunca, insan kas hücreleri, kas proteinleri kırılması ve bazik bir amino asit, alanin dönüştürerek hızlı bir şekilde uyum sağlar. Kaslar daha sonra karaciğer, sözde glukoz-alanin çevrimi olan bir değişim sistemi içeren bir yeni bir mekanizmaya dayanır. Kas proteininden türetilen alanin, kana salınır ve ekteki şekilde görüldüğü gibi, enerji üretimi için kullanılmak üzere karaciğere sevk edilir. boşaltım için böbreklere ve atık, üre verilirken Karaciğer sonra, glukoneogenez yoluyla alanin fazla glikoz oluşturabilir. Bu aynı zamanda karaciğer, kendi enerji ihtiyaçlarını karşılamak için bazı ATP rejenere olmasını sağlar, bu gibi stresli koşullarında oldukça büyüktür. Glukoz heyecanla kendisi için daha fazla ATP üretmek için o kadar sürer kas hücresi, kan akışı yoluyla sevk edilir. Glikoz anaerobik işlem de alanin dönüştürülebilir piruvat elde edilir, ancak daha başka bir enzim çalışması gerekmektedir. Piruvat, yetersiz oksijen mitokondriye gönderilemez Bu suretle, bunun yerine, bir enzim, ALT (alanin aminotransferaz) yardımıyla alanin dönüştürülebilir 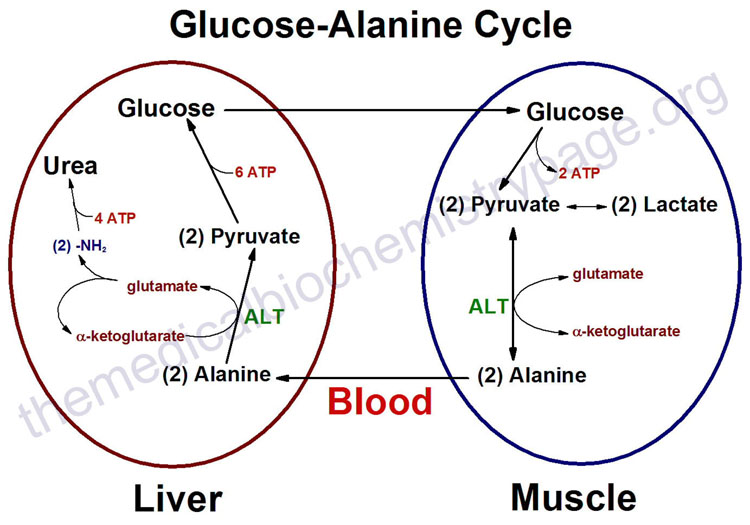 olarak uzun bir süreç içinde alfa-keto glutarat dönüştürülür glutamat, iyi bir kaynağı olarak orada.
olarak uzun bir süreç içinde alfa-keto glutarat dönüştürülür glutamat, iyi bir kaynağı olarak orada.
Yukarıdaki tartışma, çeşitli enzimler, bu sitoplazmik enerji üreten işlemleri çalışması için mevcut olması gerektiğini tespit edilmiştir. Bu kreatin kinaz, laktat dehidrogenaz, ve ALT içerir. Statin kullanan rutin olarak yürütülür adlandırılan karaciğer enzim testi kanda ALT konsantrasyonunu ölçer. Kas enzimi testleri kreatin kinaz ve kanda laktat dehidrojenaz konsantrasyonlarının saptanması. Bunlar kasları tercihen anaerobik yerine aerobik mitokondrilerde sitoplazmasında glikoz işleme olduklarını gösteren çünkü böylece bu testler bu özel enzimleri ölçüm vardır; yani mitokondri düzgün çalışmıyor. Daha sonra onu tekrar olacaktır gibi akılda bu noktayı tutmalı.
6. Aşırı Egzersiz Rabdomyoliz yol açabilir
Insanlar böyle uzun mesafe maraton koşu veya ağırlık taşıyan egzersizler gibi aşırı egzersiz meşgul, bunlar nedeniyle yeterli enerjiyi korumaya çalışırken kendi sisteminde uygulanan stres, onların kaslara ve böbrekler için hem ciddi hasara sebep olma riskiyle kasları yakıt. Bu potansiyel hasar bilinen bir göstergesi olarak kandaki kreatin kinaz düzeylerinin ölçülmesi için yaygın bir uygulama haline gelmiştir [5]. Kimin kreatin kinaz düzeyi alır hayli yüksek olasılıkla böbrek [böbrek] başarısızlığı önlemek için acil tıbbi yardım gerekecektir kişi.
Böbrek yetmezliği nedeni, rabdomiyolize, taviz veren veya ölü kas hücreleri kan akımı içine döküldü edilmiş en olası miyoglobin olup. Çok fazla miyoglobin serbest bırakılması durumunda, özellikle yetersiz su kaynağı ile, miyoglobin olarak bilinen bir durum neden böbrek filtreleme sistemi engelleyebilir “akut tübüler nekroz.” Sorunu kolayca koyu olacaktır idrar rengi gözlemlenerek saptanabilir kahverengi. 2009 yılında yayınlanan bir araştırma rabdomiyoliz olarak, böbreklere hasar miyoglobin ve böbrek hücrelerinde mitokondri arasında doğrudan etkileşimini içerir göstermiştir. Mitokondriyal membranlar elde edilen oksidasyon solunum yetmezliği ve daha sonra hücre ölümüne yol açar.
Miyoglobinüri nedeniyle genellikle rabdomiyolize, idrarda miyoglobin tanımlamak için kullanılan bir terimdir. Göre, ciddi miyoglobinüri olan hastaların% 15, akut böbrek yetmezliği geliştiren ve yüksek ölüm oranları ile ilişkilidir. Diyaliz veya intravenöz sıvılar yeterince hızlı sokulup, ya kişinin kurtarmak mümkün olmayacaktır.
Gibi erken 1991 olarak, Japon bir grup araştırmacı koenzim Q10 nedeniyle yorucu egzersiz kas hasarından sıçanları korumak için oral yoldan edilebileceğini gösterdi. Ayrıca, kontrol fareleri, öte yandan, koenzim Q10 uygulanmıştır sıçan, kreatin kinaz ve laktat dehidrojenaz seviyelerine sahip olmayan ki fark ettik.
7. Miyoglobin: İyi, Kötü ve Çirkin
Miyoglobin özel olarak oksijen yaptıkları muazzam ihtiyaçlarında kendilerine yardımcı olmak için kas hücreleri için uyarlanmış eşsiz bir proteindir. Fiziksel yapısı sağdaki resimde şematize edilmiştir. O kimin aktif (şekilde kırmızı şematize) bir merkezi heme elemanı ihtiva etmesi ile hemoglobin benzer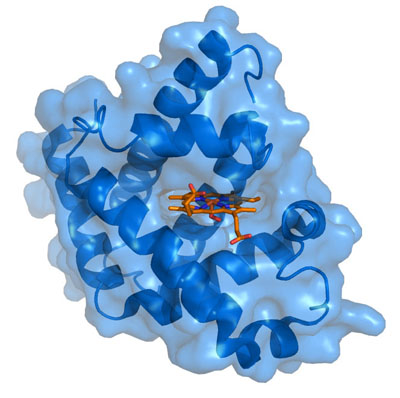 madde bir tek yüklü demir atomu (Fe) ‘dir. Kırmızı kan hücreleri içinde bulunan hemoglobin, akciğerlerden vücudun tüm dokulara oksijen taşır, miyoglobin, fonksiyonları aşırı talep dönemlerinde kaynağı tampon yardımcı, kas hücresinde aşırı oksijen depolama. Ayrıca, mitokondriya, hücre duvarından oksijen iletir. Hatta miyoglobinden yardımıyla, bu kaslar laktik asit inşa ve kan akışına salınır sırasında ağır egzersiz altında anaerobik metabolizma, başvurmak zorunda dava sıklıkla bu.
madde bir tek yüklü demir atomu (Fe) ‘dir. Kırmızı kan hücreleri içinde bulunan hemoglobin, akciğerlerden vücudun tüm dokulara oksijen taşır, miyoglobin, fonksiyonları aşırı talep dönemlerinde kaynağı tampon yardımcı, kas hücresinde aşırı oksijen depolama. Ayrıca, mitokondriya, hücre duvarından oksijen iletir. Hatta miyoglobinden yardımıyla, bu kaslar laktik asit inşa ve kan akışına salınır sırasında ağır egzersiz altında anaerobik metabolizma, başvurmak zorunda dava sıklıkla bu.
Miyoglobin Mg olarak karakterize edilebilir en az üç farklı formlarda var+2 (Demir), Mg+3 (demirli), ve Mg+ 4 merkezi demir atomuna üzerinde mevcut olan yükün miktarına bağlı olarak, (Ferryl). Mg olarak+2, sağlıklı durum, hali hazırda oksijen alma ve Mg dönüştürüldüğünde, oysa saklayın+3 bir protonun eklenmesiyle, etkisiz hale gelir. Bununla birlikte, daha başka bir proton ilavesi ile, bu Mg olur +4. Kas hücrenin dış hücre duvarında bulunan yağ asitleri de parçalamaya başlar bir yüksek derecede toksik reaktif madde (peroksidatif hasarı olarak adlandırılan) ve [ve hücre duvarında kolesterol yok etmek için devam. Miyoglobin, hidrojen peroksit gibi reaktif oksijen bileşiklerinin neden olduğu oksidatif stres altında, örneğin serbest radikaller, aşırı miktarda varlığında Ferryl miyoglobin olur. Nedeniyle koenzim Q10 yetersiz tedarik – oksijen ortadan kaldırıcı ve suya dönüştürülmesi işlemi eksik olduğu için statin tedavisi ile, hidrojen peroksit mitokondri oluşturulur, hatırlayın.
Bir hücre, oksidatif stres yaralı olan işlemi tarif mükemmel makale 1994, John Farber tarafından yazılmıştır. O yazdığı “Bütün aerobik hücreler, enzimatik olarak ya da nonenzymatically, O kurucu bir akı üretmektedir H2O2. Ve muhtemelen * OH. Aynı zamanda, pek çok hücre bol antioksidan savunma tekrar enzimatik ve enzimatik olmayan, hem de hücre yaralanmasına neden olan bu tür engeller. Bununla birlikte, kısmen indirgenmiş oksijen türlerinin oluşumunun hızı ve arttırılır/veya hücrelerin antioksidan savunma zayıflamış edildiği durumlar da vardır. Her iki durumda da, oksidatif hücre yaralanma olabilir.” Enerji üretmek için besin kaynaklarının aerob oksidasyon süreci mümkün olduğunca sitoplazmada bileşenleri korumak için mitokondri ile sınırlıdır. Ancak miyoglobin mitokondri sitoplazmadan yoluyla hücre duvarından oksijen taşıma görevlendirilmiştir. Bu oksijene maruz kalmasını önlemek ve olamaz o oksijeni teslim ettiğinde, mutlaka sonuçta suya oksijen dönüştürür işleminin bu toksik ara ürünlerle temas için yer alır. Kas hücrelerinde koenzim Q10 en önemli rollerinden biri, bu oksidatif ajanların neden olduğu miyoglobin zarar nötralize etmektir.
Bir kişinin kalp krizi (iskemik olay) muzdarip, bir koroner arterin duvarında plak bozulması aşırı yaşamaya onların kalp parçası neden akışının tıkanması ile sonuçlanabilir eksikliği oksijen. Ancak, kalp krizi sonucu en tehlikeli yönlerinden biri sözde reperfüzyon periyodu kan dolaşımı geri yüklendiğinde, ancak hücrelerin sonra oksijen yokluğundan bir sonucu olarak yaralanma uğramış. Hayatta kalabilmesi için çok önemlidir çünkü bu durum, kalp kası için özellikle sorunludur. Kalp krizi geçiren, fareler üzerinde yapılan bir çalışmada yaralanma Fe maruz doğrudan bir sonucudur olduğu ileri sürülmüştür +4 miyoglobin (ferryl miyoglobin) elde edilmiştir. Hücreler yoksunluk döneminde fizyolojik durumunu korumak mümkün olmuştur, çünkü onlar oksidatif strese karşı oldukça savunmasız.
Bir kas hücre duvarı yağ asitleri Toksik Ferryl miyoglobin maruziyet kırılmış sonra, hücre hızla parçalanır. Hücre duvarı iyonlarına artık geçirgen olduğu için, kalsiyum büyük miktarlarda hücre içine akan başlayın ve ölür kısa bir süre sonra. Ölü ve ölmekte olan hücrelerin enkaz kan dolaşımına dağınık ve bertarafı için böbrekler yolunda yapar alır. Bu girdaba doğru bazen de onların yetmezliğine yol açabilir böbrekler ve durumun şelaleleri üzerinde muazzam bir yük neden olur.
1994 yılında, Mordente ve ark. Q koenzimi oksidatif hasara ‘den miyoglobin koruyabilecek olan in vitro derecesi belirlendi bir kağıt yayınladı. Bunların sonuçları Q koenzimi miyoglobin için doğal bir antioksidan olarak çalışabilir ikna edici bir şekilde göstermiştir. Bunların özet son cümle alıntı: “Toplu olarak, bu çalışmalar, doğal olarak oluşan bir antioksidan olarak koenzim Q önerilen fonksiyonu da H azaltılması ve yeteneği ile ilgili olabileceğini düşündürmektedir H2O2 [hidrojen peroksit] miyoglobin aktive edilmiş. Koenzim Q, bu nedenle H anormal generasyonu neden olmaktadır kardiyak ya da kas bozuklukları hafifletmelidir H2O2“.
Kolesterol Enerji Membranlar Korur ve Kaydeder Nasıl 8.
Memeli hücreleri kolesterol olmadan yaşayamaz. Kolesterol, vücuttaki tüm hücreler dış duvarı (hücre membram) bulunur. Ayrıca mitokondri ve lizozomlar (sindirim ileri derecede asitli kaplar hem çevreleyen iç zarlarında bulunan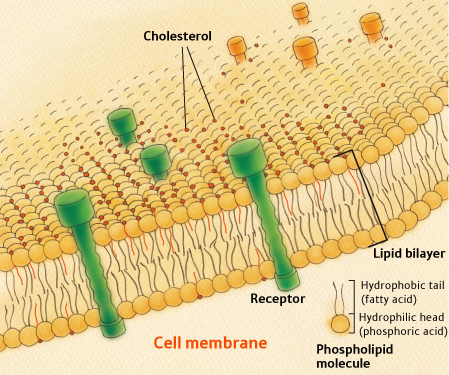 enzimler). Kolesterol nasıl çalıştığını anlamak için, hücre zarının yapısı hakkında bilgi vermek gerekir. Sağdaki şekilde gösterildiği gibi tüm hücre zarları, sözde çift katlı lipid inşa edilir. Lipid iki katmanlı fosfolipid (LDL parçacıklarının, sözde “kötü” kolesterol örten aynı fosfolipidler) iki paralel zincir içerir. Fosfolipidler, molekülün bir ucu hidrofobik olduğu gibi özgün bir özelliği (suda çözünür) ve diğer hidrofilik olan (suda çözünür). Lipit çift katman içinde iki zincir maddeleri bu her iki tabakada hidrofobik kenarları membranın merkezi bitişik olduğu yönlendirmek. Bu merkezi bir hidrofobik katı, bu nedenle oksidatif hasara karşı hassas olan yağ asitleri içerir. Dış ve hücrenin iç hem bakan dış parçalar, suda çözünürdür.
enzimler). Kolesterol nasıl çalıştığını anlamak için, hücre zarının yapısı hakkında bilgi vermek gerekir. Sağdaki şekilde gösterildiği gibi tüm hücre zarları, sözde çift katlı lipid inşa edilir. Lipid iki katmanlı fosfolipid (LDL parçacıklarının, sözde “kötü” kolesterol örten aynı fosfolipidler) iki paralel zincir içerir. Fosfolipidler, molekülün bir ucu hidrofobik olduğu gibi özgün bir özelliği (suda çözünür) ve diğer hidrofilik olan (suda çözünür). Lipit çift katman içinde iki zincir maddeleri bu her iki tabakada hidrofobik kenarları membranın merkezi bitişik olduğu yönlendirmek. Bu merkezi bir hidrofobik katı, bu nedenle oksidatif hasara karşı hassas olan yağ asitleri içerir. Dış ve hücrenin iç hem bakan dış parçalar, suda çözünürdür.
Kucerka ve arkadaşları tarafından 2009 yılında yayınlanan bir makale. Kolesterol, bütün hayvan hücre zarlarında bulunan”ve uygun membran geçirgenliği ve akışkanlık için gereklidir: güzel zarlarında kolesterol bilinen çeşitli roller özetliyor. Aynı zamanda, hücre zarlarını bina ve muhafaza edilmesi için gerekli olan ve bir antioksidan olarak hareket edebilir. Son zamanlarda, kolesterol hücre sinyal süreçlerine dahil edilmiştir, ve plazma zarı içindeki lipid salı oluşumunu sağlamak için önerilmektedir.” Madde (membran lipid tabakasının hidrofobik bir iç boşluk içinde tecrit) kolesterol yatay (membran boyunca köprü) ya da dikey olarak zarın içinde kendini yönlendirmek mümkün ya da açıklamak için devam eder. Nasıl yönlendirilmiştir, membranda doymuş yağ asitleri olan derecesine bağlıdır doymuş yağ asitleri, büyük ölçüde yatay bir yönelimde üzerine dikey lehine olan. Kolesterol aynı zamanda diğer çift-katlı bir tarafından kolaylıkla çevirebilirsiniz. zarı içinde yönlenmesinden bu esneklik bakıldığında bu sinyal molekülü olarak etkili bir çalışmasına olanak sağlar.
2001 Thomas Haines tarafından yazılan bir makalede, ilginç sodyum sızıntı ‘den, hücre membranını korumaya kolesterol için yeni ancak zorlayıcı bir rol önermektedir. Tüm memeli hücreleri, hücre kimyasal işlemleri yakıt kullanılır dış duvar boyunca bir iyon gradyanı sürdürmek. Adlandırılan sodyum pompası sürekli bu yük farkı sürdürmek amacıyla, hücrenin dışına sodyum pompalar aktif bir süreçtir. Pompa sürecinde ATP tüketir. Pompa karşı çalışma geri hücre içine kayması sodyum neden olan bir pasif kaçak mekanizmadır. Membran (tür bir evin tavan izolasyon koyarak gibi) sızıntı direnç gösterecek şekilde inşa edilebilir ölçüde, hücre düzgün çalışması için uygun bir sodyum konsantrasyonlarını korumak için daha az ATP gerektirecektir.
Haines madde kolesterol sodyum kaçak hücre duvarı korunmasında önemli bir rol oynadığını ileri sürer. Sodyum sızıntı doymuş yağlı asitler gibi doymamış yağ asitleri için çok daha büyük bir problem (kolesterol yokluğunda hızlı 7 ila 11 kat sızıntıları) ‘dir. Bununla birlikte, doymamış yağ asitleri de merkezi tabakanın kendisini düzenlemek için kolesterol ediyoruz. Orada birikerek, bu pasif hücrenin iç dış atlamalı şarj sodyum iyonları önlenmesi ilave yalıtım sağlar. Diğer deneyler göre sodyum sızıntı oranları kolesterol varlığında 300% azalma olduğunu göstermiştir.
9. Kaslara Statin Hasar Kanıtlar
Eğer kişi Bir stres testi başarısız olursa ya da kalp krizi uğrar ve Genellikle Amerika’da, bloke edilmiş bir koroner arter sahip olduğu bulunmuştur, yani bir stent beklentisi ile, problem ve yüksek doz statin tedavisi başlatılacaktır doğru tanıtılacaktır ilaç onların hayatının geri kalanı için ihtiyaç olacağını. Kabul inanç bugün olursa olsun kolesterol zaten düşük olup olmadığını, yüksek doz statin tedavisi bu durumun neden olduğu yan etkileri dengelemek için yeterli faydayı sağlayacak olmasıdır. Aynı zamanda, bu hastalar egzersiz kalp hastalığı prognozu için oldukça yararlı olduğu görülmüştür, çünkü bir koşu bandı üzerinde egzersiz günde bir saat kadar harcamaya teşvik edilmektedir. Egzersiz, statin ilacı ile uyarılan metabolik bozuklukları ile bağlantılı olarak, potansiyel olarak ölümcül bir bileşimidir.
Tipik olarak, aynı zamanda, hasta statin ilaçların yaygın bir yan etkisi, kas ağrısı ve kas zayıflığı olduğu uyarı yok. Genellikle bu tür belirtiler hemen görünmez durumdur. Statin tedavisinin belirgin belirtileri neden olacak kadar hasar neden önce Aslında, bazen yıllar olabilir. O zamana kadar, kişi de ağrı ve halsizlik basitçe eski almanın bir sonucu olduğuna inanıyoruz olabilir.
Bu yaygın talep edilmişse ve statin kullanıcıları size enzim düzeylerinin izlenmesi sürece, enzimler çok yüksek alırsanız sadece statin tedavisine kesebilirler ve her şey iyi olacak, yani bu kavramı benimsemiş görünmektedir. Ancak, tüm web üzerinden açıklama sayfalarında gösterildiğinden üzücü hikayelerinden bazıları bakarsak, bu bazı insanlar için durum olmamaya dönüştü.
Temmuz 2009 yılında yayınlanan bir makalede, fiziksel kası hasarı ve kas zayıflığı ya da ağrısı hastaların şikayetleri arasındaki ilişki incelenmiştir. Zayıflık bildirdi Hastalar kol desteği olmadan oturduğu yerden kalkmak zor olduğunu, örneğin, dedi. Genellikle ağrı bildirdi olanlar fiziksel egzersiz sonrası daha kötü olduğunu söyledi. 44 hastanın sadece bir takım 57.657 U/L ölçülen kas enzimi kreatin kinaz serum düzeyi ile, belirgin rabdomiyoliz geliştirilmiştir incelenen. Onun ağrı tedavisinde Bu hasta gerekli hastane tedavisi.
Yazarlar hangi kas hasarı Bu hastalar için kas biyopsisi yoluyla görülebilir kapsamını, ilgilenmişlerdir. Onlar bir statin ilacı almamış 20 hasta ile karşılaştırdı. Statin alan 44 hastanın yirmi beş berrak kas hasarı oldu. 20 kontrollerin hiçbiri hasar herhangi bir kanıt yoktu. Bunların elyafların ortalama 10% yaralandı üzerinde aşırı rabdomiyoliz olan bir hasta dışında, diğerlerinin hiçbiri, üst düzey “normal”. yaralanması olan hastalar için kabul sınır noktasının üstündedir ve kas enzim seviyelerine sahip olmuştur. Yazarlar kreatin kinaz düzeylerinin yükselmesiyle eksikliği yapısal kas yaralanması dışlamadığına sonucuna varmıştır.
10. Statinler ve Kalp Yetmezliği
Kalp bir kastır ve dolayısıyla tüm tabidir “Bu Koenzim Q10 kalp fonksiyonu için vazgeçilmez olduğunu kurulur.”: basitçe başlıklı kağıt soyut olarak tümden devletler “Lovastatin insanlarda koenzim Q seviyelerini düşürür” iskelet kaslarının olarak fizik aynı kanunları. Bu nedeniyle statinler, yukarıda tartışılan metabolizmasına sahip olan çeşitli etkilere yakıt eksikliği aynı sorun ile karşı karşıyadır. Kalp kası hücreleri de yeterli yakıt almak için kendilerini yediklerini olurdu ve ayrıca Ferryl miyoglobin maruz kalma nedeniyle hücre zarlarında hasara uğrayacaktır.
2004 yayınlanan bir makalede kalbinde kas hücreleri kalp yetmezliğine yol açarak, yaşlılık ile işlevsiz hale işleme ilişkin makul teori sağlar. Argüman hasar hücrelerini statinler hangi mekanizma ile ilişkili mantıksal kesintiler ile mükemmel uyum ve statinler bir ivmeyle yaş yapmak kaçınılmaz sonuca yol açar. Işlem mitokondri ve lizozomlar hem de yetersizliğinin neden olduğu aşağı doğru bir döngü bulunmaktadır. Mitokondri hücre yakıt sağlanması için sorumludurlar ve lizozomlar sindirilmesi ve artıkların kalıntıları dekompoze sorumlu olduğunu hatırlayın. Madde aşağıya doğru spiral neden olduğu iddia “sürekli fizyolojik oksidatif stres”. Oksidatif stres çok statinler geliştirilir, Onlar hasarlı hücre duvarlarını yeniden inşa etmek için koenzim Q10 ve taze fosfolipid ve kolesterol gibi hem antioksidan nedeniyle dolabilir çünkü. Hücre duvarının zarar fosfolipidlerden Moloz mitokondriyal duvarlar ve lizozom duvarlar, lizozomlar tarafından alınan sindirilir ve atılmalıdır. Normal şartlar altında lizozomlar kolayca güçlü sindirim enzimleri kullanarak, onların yüksek asitli ortamda onları yıkmak olacaktır.
lizozomlar hasarlı hücre duvarlarından biriken çöpleri sindirimi mümkün olduğunda, geri kalan kalıntı “lipofusin” olarak adlandırılır. Lipofusin yaşlılık ait bir işaret olarak kabul edilir, karaciğer, böbrek, kalp kası ve sinir hücrelerinde biriken yaşlandığımızda. Lipofusin doymamış yağ asitlerinin oksidasyonu ürünü olduğuna inanılmaktadır olup olmadığı ve hücrenin dış duvarına veya lizozomlar ve mitokondria duvarlarına, zar hasan göstergesidir edilir.
Lizozomlar işlevsiz olduğu için uzun süreli statin kullanıcıları için, lipofusin neredeyse kesinlikle, biriktirir. Bu durum sadece kalbinde değil ortaya, ama vücudun tüm hücrelerinde olur. Daha önce de belirtildiği gibi, statinler dolikoller, korunmasında önemli bir rol oynamaktadır antioksidan üretimini sakat lizozomlar, hidrojen iyonu sızıntı. Lizozomlar ayrıca bağlı kolesterol şarj dağılımı karşı ilave yalıtım sağlamak için kendi zarlarında. Dışarı doğru H sabit bir sızıntı ile + iyonları, lizozomlar enzimleri çalışmasına izin vermek için yeteri kadar asidik bir seviyede pH değerini muhafaza edilemez. Sonuç olarak, undegradable enkaz, yani lipofusin olarak lizozomlannda biriktirir ve hücre felaket kurtarma hiçbir yedekleme onarım sistemine sahiptir. Ozetinde son sözünün diyor ki: “Bu birbiriyle mitokondriyal ve lizozomal hasar sonunda fonksiyonel yetmezliği ve kardiyak miyositler {kalp kası hücreleri] ölümü ile sonuçlanır.”
Doktor Peter Langsjoehn statinlerin kalp yetersizliği görülme sıklığında bir salgın artış uyaran olduğuna inanmaktadır. Şöyle diyordu: “Tyler, Teksas 17 yıl benim Uygulamada, ben, kullanım statin sekonder kalp yetmezliği korkutucu bir artış gördük ‘statin kardiyomiyopati.’ Son beş yıl içinde, statinler daha güçlü hale gelmiştir, daha yüksek dozlarda reçete ediliyor ve pervasız yaşlılarda ve ‘normal’ kolesterol düzeylerine sahip hastalarda terk ile kullanılmaktadır. Biz son on yıldır dramatik bir artış ile ABD’de bir CHF salgını ortasındayız. Biz statinlerin bizim gayretli kullanımı yoluyla bu salgına neden musunuz? Büyük oranda Cevabın evet olduğunu düşünüyorum.” (Statinler ve Kalp Yetmezliği).
Dr Duane Graveline, statin tedavisinin tehlikeleri uzun süredir savunucusu, çok net bir açıklama sağlamıştır (Statinler üzerinde Duane Graveline ve Kalp Yetmezliği) kalbinde koenzim Q10 rolünün ve bunun nedenini statinler tarafından inhibe olur kalp yetmezliğine yol açabilir. Sen o sayfada Dr. Langsjoehn tarafından ilgili maddelerinde çeşitli başvurular bulabilirsiniz.
Çok yeni bir çalışmada (Kasım 2009) olan hastalar tespit diyastolik statin alan kalp yetersizliği statin tedavisi olmayan hastalara göre anlamlı derecede daha kötü bir sonuç vardı. Diyastolik kalp yetmezliği bu dinlenme fazı yerine sözleşme aşamasında kalp fonksiyon bozukluğu ile bağlantılı olduğu sistolik kalp yetmezliği ayırt edilir. Ancak, kalp yetmezliği vakalarının yaklaşık yarısının nedeni olduğunu ve sistolik biçimi olarak eşit olarak ölümcüldür. Çalışmada statin tedavisi idi diyastolik kalp yetmezliği olan kişilerin akciğerleri ile ilgili sorunlar daha fazlaydı ve kendilerini değil statin dışındaki (zayıf kaslar, yoksul egzersiz toleransı) uygulamak için daha az yetenekli olduğu doğrulandı.
11. Statinler ve Akciğer Hastalığı
Statin sanayi statinler olabilir fikrini teşvik etmeye çalıştı yararlı zatürre tedavisinde. Onlar gözlenen faydaları statinler aldı olanlar statin tedavisi tanıtmadan önce muhtemelen uzun yıllar boyunca yüksek kolesterol yararlanmıştır olmasından kaynaklanıyordu, sanıyorum, gel retrospektif çalışmalar aracılığıyla bu hatalı sonuca vardık. Sanayi yeterince sonra iddialarını meşrulaştırmak için denemek için plasebo kontrollü çalışmalar yapmak üzere ön olumlu göstergeler tarafından teşvik edildi. Açıkça statin tedavisi yararlı değildi sadece gösterdi, ama aslında önemli ölçüde daha kötü prognoz yol açtı Ancak, çalışmalar, tepti (bkz (Statinler Pnömoni Riskini artırın). Hastaneye yatmayı gerektirecek kadar şiddetli pnömoni, bir statin alarak tarafından yapılan riski endişe verici 61% idi.
kaslar Statinlerin etkileri elbette daha da zatürre ve kalp yetmezliği hem ağırlaştırmaktadır, nefes almada zorluk ve müteakip oksijen yoksunluğu, yol, hem de solunum kaslarının için geçerlidir. Bundan başka, şimdi de nadir durumlarda, statin ilaçlan, şiddetli akciğer hastalığına neden “interstisyel akciğer hastalığı” (ILD) olarak adlandırılan, bilinmektedir. İAH artık tüm statin ilaçlar için nadir bir yan etki olarak listelenir.
2008 yılında yayınlanan mükemmel bir derlemede, Fernandez ve ark. Statinlerin interstisyel pnömoni neden olabilir nasıl çok sayıda olanak tanımak. Bunlar, amiodaron ile bir analoji çizerek tartışma başlar, bilinen bir ilaç bölümde tarif edilmiştir lizozomal Dahil etme gövdelerinin birikmesini içerir patolojinin oldukça benzer bir tür, yani lipofusin, hücre membran döküntü neden kalp hastalığı altında.
Amiodaron “amfifilik” ilaç olarak bilinen ilaç çok yaygın bir sınıfa ait: bir hidrofilik (suda çözünür) ve bunların kimyasal yapısında lipofilik (yağ çözünür) bileşeni de bulunmaktadır. Bu özellik onların arzu biyokimyasal etkilerini elde etmek için hücrelerin zarları yoluyla geçmeye olanak tanır. Ancak, hücreye girmesi bir süreçtir hücre membranı lipitleri bozundurucu içerir. Membran fragmanları hücre çeperinden uzağa kırmak ve hücre içine onlarla birlikte ilacı taşırlar. Hücre duvarı bozulma bir sonucu olarak, sodyum sızıntıları hücre önce tarif edilmiştir tüm olumsuz sonuçlarla birlikte, enerji kaybetmesine neden olacaktır.
Fernandez vd. bunlar bir apolar (lipofilik) halka ve bir hidrofilik yan zincire içeren bu yana amiodaron gibi, statinler, amfifilik bir yapıya sahip, iddia etmektedir. Yaptıkları Gerçekten rahatsız gözlem zamanla amfifilik ilaçlar hücrelerin giren daha verimli hale bilinmektedir, olmasıdır. Bir bozulan hücre duvarı ilaç molekülüne daha iyi geçirgenliği sağlayacak mantıklı görünüyor. Ama bu daha sonra uyuşturucu hücre üzerinde ne varsa etki hızlandırılmış hasar ve yıkıcı bir çağlayan yol artar olacağı anlamına gelir.
Amiodaron güçlü bir antidysrhythmic madde, yani, kalp yetmezliği ya da ameliyat sonrası sırasında düzensiz kalp atışı düzeltmesi kullanılan bir ilaçtır. Bu çok sayıda yan etkileri vardır, ancak muhtemelen en ciddi yan etkisi interstisyel akciğer hastalığıdır. 2001 yılında yazılan bir makalede pulmoner hasarın muhtemel mekanizmasını araştırdı. Akciğer dokusunda hücreler üzerinde in vitro deneylerde yapılan yazarlar hamster ekstre edilmiştir. Bu ilaca maruz kalma mitokondriyal membran potansiyeli (lH azaldığı not + iyonlar 32 ila 77% oranında düşmüştür hücrede daha sonra ATP miktarı mitokondri dışarı sızdırılmış) ve benzerleri. Hatta glukoz ilave edilerek, mitokondri tükenmiş ATP yeniden mümkün değildi; yani mitokondri glikozdan enerji üretmek için düzgün değildi. Sonuçta, hücreler öldü. Bu mitokondriyal fonksiyon bozukluğu, ilaç hücre ölümüne neden hangi yol olduğu sonucuna vardık.
Ne tarif esasen statinlerin kas hücrelerinde sorunlarına yol açtığı tam olarak aynı işlemdir. Fernandez vd. amiodaron gibi, statinler mitokondriyal elektron taşıma zinciri ve ATP müteakip tükenmesi onların bozulması suretiyle interstisyel akciğer hastalığına neden olabilir, tezimin katılıyorum. Havadaki oksijen yakalama ve kana Taşımadan görevli olduğundan akciğer hücreleri, özellikle oksidatif hasara karşı hassastır. Ben de bildirildi intersitisyel hastalık vakalarının sayısı az olmasına rağmen, akciğerler, pulmoner fonksiyon henüz feci noktaya kötüleşti değil statinler, fakat tarafından ele geçirilmiş insanlar çok daha büyük bir sayı yoktur, şüpheleniyoruz. Bunun yerine, bazı zorluk nefes ve yeteri kadar oksijen almak için algılanan yetersizlik yaşamaktadır. Kas zayıflığı gibi, Hasta o ne yaşanıyor eski büyümenin normal bir yönü olmadığını bilmenin bir yolu vardır gibi belirtiler bildirilmemiş gidebilir. Akciðer hücreleri yetersiz enerji ve bozulmuş hücre duvarından acı çekerken Kesinlikle viral pnömoni artan duyarlılık beklenebilir.
12. Statinler ve Diyabet
Statin ilacı Rosuvastatinin JUPITER çalışması yaygın statin ilaçlar C-reaktif protein denilen inflamasyon göstergesi yüksek düzeyde olan insanlar için kalp krizi geciktirebilir delil olarak takdim edildi. Ancak, ne az bu deneme hakkında bilinen bu statin ilaçlarının (ya da en azından rosuvastatin) ve diyabet riski arasında açık bir bağlantıyı ortaya çıkardı olmasıdır (JUPITER Yargılama ve Diyabet). Dr Jay Cohen göre, deneme rosuvastatin aldı insanlar kontrol grubuna kıyasla, gelişmekte olan diyabetin 25% riski vardı. Diyabet kendisi kalp hastalığı için son derece güçlü bir risk faktörüdür, çünkü bu, endişe verici.
Pankreas beta hücrelerinde insülin sentezler ve insülin üretimindeki kusurlar (de bunun az ya da buna yanıt eksikliği ya) diyabetin nedenidir. İnsülin glukozu hücre içerisine taşınmasını katalize vücudun hücreleri tarafından kullanılır. İnsülin olmadan, ya da kötü insülin işleyen ile, şeker kanda yukarı yığınları ve hücreler enerji hasret olur.
Orada beta hücreleri ve ensülin üreten makine biyokimya çalışmaların büyük bir sayı olması, ve beta hücreleri kolesterol ve yağ de insülin serbest önce mevcut olduğu her iki ihtiyaç olduğu tespit edilmiştir. Beta hücrenin dış zarı içinde yetersiz kolesterol ve kalitesiz fosfolipidler olasılıkla zar boyunca insülin taşıma yeteneğini bozar. Bu statinlerin bastırmak aynı LDL parçacıklarının yoluyla kan akımı içinde taşınmaktadır için statin ilaçlar, tabii ki, aynı zamanda yağ asitleri, kolesterol biyo azaltır, ancak. Böylece, statinlerin şeker hastalığına riski neden neden görmek kolaydır.
Hücre zarındaki yukarıdaki kusurlar ek olarak, beta hücrelerinde mitokondri bozulmuş fonksiyonu da açık bir şekilde kusurlu mitokondriyal genlerin ile diyabetik fareler içeren çalışmalarda, diyabette rol oynar. sadece beş haftalıkken Bu fareler düşük insülin salgılanması gösterir ve bunların mitokondri görünüm anormal ve bunların membranlar boyunca yeterli bir yük gradyanı sürdürmek üzere, yapamaz. Başka bir deyişle, onlar statin maruz kalma sonucu düşürülmüş koenzim Q10 ile beklenenin benzer kusurları sergiledi. Bunların pankreatik beta hücrelerinin pek çok kapalı ölmüştü aynı defektli yaşlı farelerin, insülin üretiminde ciddi eksiktir.
İnsülin yağ hücreleri ve karaciğer hem yağ salınmasını bastırmaktadır ve bol miktarda yağ hali hazırda mevcut olmadıkça, bu nedenle, insülin salgılanmasında sonra kan akımı içinde bir yağ sıkıntısı olacaktır. Beta hücreleri emin yağlar ve kolesterol de kan akışına insülin enjekte etmeden önce temin edilir olmak için Böylece, biyolojik, iyi bir stratejidir. Daha önce bu konuda kapsamlı yazdım (Metabolik Sendrom Açıklaması).
[41] Mart 2009 yılında yayınlanan bir çalışmada statin ilacı kullanımı ve açlık kan şekeri seviyeleri arasındaki ilişkiye bakmış, testi genellikle şeker hastalığı riskini değerlendirmek için yaptık. Bunlar iki kategoriye ayrılır 345.417 hasta gruplandırılmış: ile veya önceki diyabet tanısı olmadan. Onlar statin alan başlamış ve daha sonra iki yıllık ortalama statin olmuştu sonra önce onlar açlık glukoz düzeyleri karşılaştırıldı. Her iki grupta da, bunlar statin tedavisi olanlar için artan açlık glikoz seviyelerinin yüksek (P <0.0001) ve sonuçları elde edilmiştir.
İnsülin arzındaki azalmaya dolaylı kas hücrelerine girmek için glikoz yeteneğinde bir azalma, kusurlu bir aerobik metabolizma fabrika hayatta kalmaya çalışan kas hücreleri için yaralanma üzerine hakaret eklersiniz. Kaslar oksidatif hasarı önlemek için glikoz çok daha az verimli anaerobik metabolizma geçmek zorunda olduğundan, onların mitokondriyal enerji üreten fabrika düzgün yapılsa gerektirecektir daha enerji arzını karşılamak için muazzam fazla glikoz gerektirir. Oysa azaltılmış insülin zor yeterli glikoz almak için yapıyor. Bu iç kas proteininin cannibalization yol açar açlık moduna hücreyi zorlayacaktır. Zamanla algılanan sonuç aşırı kas zayıflığı olacaktır.
13. Sonuç
ABD’de yaşayan ve doktorunuz size kalp krizi, yüksek risk altında olduğunu tespit etti, o büyük olasılıkla kolesterol düzeyleri yüksek olmasa bile yüksek doz statin reçete etmiştir. Büyük olasılıkla da bir düşük yağ, düşük doymuş yağ diyeti geçirildi ve her gün bir koşu bandı üzerinde çalışmak için teşvik edilmiştir.
Araştırmalarım Eğer titizlikle doktor tavsiyesi tüm izlerseniz, er ya da geç şiddetli kas hasarını karşı karşıya olacak, belirtir. Mitokondri ve kas hücrelerinin hücre duvarlarında statin ilacın etkisi bile mütevazı egzersiz rabdomiyoliz yol açabilir şekildedir. Bazıları için bu yan etkileri çok zarar verici ve statin tedavisi sonlandırılmalıdır olduğu hemen aşikar olacaktır. Diğerleri için, hasar daha sinsice gerçekleştirilecek ve statin tedavisi sonrası yıllar başlayana kadar belirgin hale olmayacaktır. o kas hasarı onarmak için çok geç olacak – Ama çoğu zaman hasta belirtilerinin ilaç durdurulduğunda sonra kalan göreceksiniz. Ya da daha kötüsü, onlar bir sonucu olarak böbrek yetmezliği veya kalp yetmezliği gelişecektir.
Statin ilaçlar pek çok olumsuz yan etkileri vardır, ancak muhtemelen en sık şikayetler endişe kas ağrısı ve kas zayıflığı. Bu denemede, bu yan etkiden sorumlu mekanizma fizyolojik bir açıklama geliştirdik. Statinlerin sadece kolesterol sentezi müdahale olmasından kaynaklanmaktadır, aynı zamanda koenzim Q10 ve dolikoller. Statinler, aynı zamanda, hücreler, bu temel besin sağlayan LDL serum seviyelerinde keskin bir düşüş için, her ikisi de yağ asitlerinin hücre ve tüm diyet antioksidanlar biyolojik azaltır.
Yeterli koenzim Q10 olmadan, kas hücreleri, kasılmalar yakıt enerji üretmek için zarar görmüş bir yetenek muzdarip. Onlar hayatta kalmak için kendi proteinlerini yediklerini zorlanmaktadır. Aynı zamanda, güçlü oksitleyici maddeler oluşturulacak zarar veren hücre içinde miyoglobin, her iki etkisiz hücre çeperine oksijen ve toksik taşıma hale getirir. “Ferryl miyoglobin” olarak bilinen oksidize miyoglobin, hücre duvarının temel bileşeni yağ asitleri için toksiktir. Hücre duvarının yetersiz kolesterol ile, cep şarj tutamaz ve bu da enerji israfına neden olur. Lizozomlar bunlar yeterince asidik bir ortam sağlamak çünkü enkaz sindirimi mümkün değildir. Sorun ayrıca kolesterol derin sıkıntısı ile birleşir bu yağ asitlerinin oksidatif hasar ve iyon kaçak hücre duvarındaki, mitokondriyal duvar ve lizozom duvara daha fazla koruma teklif olurdu. Sonunda hücre ayrışan ve miyoglobin, kan akışına salınır. Bu şekilde imha deneyin böbrekler, yolunda yapar. Ama Ferryl miyoglobin de şiddetli böbrek hastalığına yol açan böbrekler, için toksiktir.
Düşük yağlı diyet ve egzersiz rejim statin ilacı sorunlara neden ihtimalini artıracaktır hem. Düşük yağlı diyet daha da hasarlı hücre duvarlarını yerine yağ asitlerinin biyoyararlılığını azaltır ederken Dinç egzersiz, kasların enerji ihtiyaçlarını artırmaktadır. Bundan başka, doymamış yağ oluşan hücre duvarları doymuş yağ oluşan daha Ferryl miyoglobin saldırılarına karşı daha hassastır.
Kalp ayrıca bir kas olduğu için, o da hasardan dolayı statinler maruz kalma uğrar. Bu diyastolik kalp krizi ve kalp yetmezliği gelişimi açısından artmış şans sonrası iyileşme açısından daha az ihtimal yol açar. Zayıf bir kalp ile birisi için çok tehlikeli her ikisi de zatürre ve interstisyel akciğer hastalığı hem riskinin artmasına solunum sistemi kurşun Hasarlı hücreler.
JUPITER çalışması tedavi grubu diyabet 25% artmış risk altındadırlar ve bu doğru olurdu neden yukarıda anlattığım ortaya koydu. Diyabet, kalp hastalığı için önemli bir risk faktörüdür, bu nedenle bu sonucun rahatsız edici ve bir deneme bu sayı daha da kötüsü yapmamak için erken sonlandırıldı olmadığını merak ediyor. Dr William Davis, statinlerin kalp hastalığı tedavisinde son çare olması gerektiğine inanmaktadır bir kardiyolog, bu JUPITER deneme şöyle aktarmaktadır: “Ben tam yararlanarak olarak halka üzerinde JUPITER argüman yoluyla Rosuvastatinin foisting görmek yağ alımını azaltın daha sağlıklı tahıl yemek ve: çaresiz durum birçok Amerikalının içinde bulurlar. . . kolesterol ve CRP Skyrocket! ‘Sen rosuvastatin gerekiyor! Bunun genetik olduğunu söylemiştim,’ güzel AstraZeneca sponsorluğunda ilaç yemeği katıldıktan sonra doktor diyor.” (JUPITER Dr. Davis’ Blog Yayını)
Haber sadece bile çocukların artık yüksek kolesterol için test edildiğini çıktı ve onların kolesterol seviyelerini kontrol edemez eğer bir statin ilacı koymak gerektiği savunulmaktadır ediliyor (Çocuklar ?? statin alan). Bu haber kontrollü statin çalışmalarından hiçbirinin çocuklar üzerinde yapılmıştır, özellikle de son derece rahatsız edici buluyorum. Biz statin ilaçları olumsuz sonuçları bir çocuğun gelişmekte olan sinir sistemi üzerinde olabilir ne hiçbir fikrim yok. Bununla birlikte, statinlerin tamamen bir embriyo sinir sistemine zarar veren göstermiştir edilmiştir.
Dikkate değer bir son Jeff Cable tarafından yayın (Aralık 2009) hastalar tarafından statin tedavisinin 885 kendinden bildirilen yan etkilerin bir dizi analiz eder. Raporlar kognitif bozukluk, kas ağrısı ve zayıflığı, cilt problemleri ve cinsel işlev bozukluğu dahil Statinlerin bilinen yan etkileri, geniş bir yelpazede kaplı olmasına rağmen, en çok ne rahatsız edici ciddi nörolojik hasar raporlarının sayıda idi. En üzücü o ALS yılında 18 olmak üzere toplam vermek, sinir hücreleri erimeye veya ölmek birlikte 1 olarak sayar motor nöron bozulması, ilgili 2 ek raporlarla ALS 17 raporların toplam vardı olmasıydı ve can artık kaslara mesaj göndermek. Bu sonuçta kas zayıflaması, seğirmesi ve sonuçta felç yol açar. Hastalık ilerledikçe, yutma ve zor hale bir solunum. Çoğu mağdur tanı beş yıl içinde ölmektedir.
Nörolojik bozukluklar ve ALS ile ilgili yazarın Buraya eklenen yorumlardan cinsindendir: “Hasta hesaplarından elde edildi bilgilerden biri parçası iyi statin tedavisi ile çöktürülmüş olabilir majör nörodejeneratif hastalıkların belirgin insidansı olduğunu. … Bu koşulların en nadir (insidans istatistiklerine dayanarak) öngörüde bulundu beklenen 3600000 hesapları onsekiz ALS/MND durumlarda önce yazılacak olurdu olacak kadar vaka ortaya çıktı sadece 351 raporlarında henüz ALS ve olur ortaya konmuştur. Bu vakaların bir şaşırtıcı yüksek sayı temel bir hata yapılıp yapılmadığı konusunda sormak doğru olur böyle küçük katılımcı grup içinde rapor şekildedir. Gerçekten neler oluyor: sormak da doğru herhangi hatası nedeniyle eksik? Ne statin tedavisi oluşturduğu gerçek bir risktir?”
FDA’nın advers olay raporlarının bir çalışma yanı sıra yüksek kolesterol ALS karşı koruduğunu gösteren bir çalışma – statin ve ALS arasında bir ilişki karıştığı literatürde önceden kanıtlar vardır. Bir sonraki deneme sinir sistemi üzerinde ilaçların muhtemel yan etkileri statin konusunda olacaktır: Ben iddia edeceğini ALS ama multipl skleroz, Parkinson hastalığı ve Alzheimer değil sadece statinlerin riskini artıracaktır.
Teşekkür
Ben kendi mükemmel yorumu kağıt ve statin hasar için benim argümanlar önemli bir rol oynamıştır lipit katları ile proton ve sodyum sızıntıları üzerinde Haines tarafından çok bilgilendirici ve ilginç yazısı, hem beni işaret için Glyn Wainwright teşekkür etmek istiyorum kaslar.